Giáo án powerpoint còn gọi là bài giảng điện tử, giáo án điện tử, giáo án trình chiếu. Powerpoint Giáo án Hóa học 7 Chân trời sáng tạo được tailieukhtn.com biên soạn dựa theo công văn mới nhất với nhiều phong cách khác nhau, hiện đại, tinh tế và đẹp mắt tạo sự thích thú cho học sinh.
MỘT SỐ TÀI LIỆU QUAN TÂM KHÁC
Click vào ảnh dưới đây để xem giáo án rõ
XEM VIDEO VỀ MẪU POWERPOINT GIÁO ÁN HÓA HỌC 7 SÁCH CHÂN TRỜI SÁNG TẠO
Chủ đề 2: PHÂN TỬ
BÀI 7: HÓA TRỊ VÀ CÔNG THỨC PHÂN TỬ
Môn học: Khoa học tự nhiên lớp 6
Thời gian thực hiện: 04 tiết
MỤC TIÊU
Về kiến thức
– Trình bày được khái niệm về hóa trị. Cách viết công thức hóa học
– Viết được công thức hóa học của một số chất và hợp chất đơn giản thông dụng.
– Nêu được mối liên hệ giữa hóa trị của các nguyên tố với công thức hóa học
– Tính được phần trăm nguyên tố trong hợp chất khi biết công thức hóa học của hợp chất
– Xác định được công thức hóa học của hợp chất dựa vào phần trăm nguyên tố và khối lượng phân tử
Về năng lực
a) Năng lực chung
– Tự chủ và tự học: Chủ động, tích cực tự tìm hiểu về khái niệm hóa trị, cách tính hóa trị, công thức hóa học, quy tắc hóa trị, công thức tính phần trăm của nguyên tố trong hợp chất, phương pháp tìm công thức hóa học dựa trên % nguyên tố và khối lượng phân tử.
– Giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để diễn đạt về hóa trị trong hợp chất cộng hóa trị, hoạt động nhóm một cách hiểu quả theo đúng yêu cầu của giáo viên, đảm bảo các thành viên trong nhóm đều tham gia và trình bày báo cáo tốt
– Giải quyết vấn đề và sáng tạo: Giải quyết vấn đề kịp thời với các thành viên trong nhóm để thảo luận hiệu quả và hoàn thành nhiệm vụ học tập tốt nhất
b) Năng lực chuyên biệt
– Nhận thức khoa học tự nhiên: Trình bày được khái niệm về hóa trị, cách tính hóa trị của nguyên tố trong một hợp chất cộng hóa trị. Trình bày được cách viết công thức hóa trị; Viết được công thức hóa học của một số chất và hợp chất đơn giản thông dụng. Nêu được mối liên hệ giữa hóa trị của các nguyên tố với công thức hóa học.
– Tìm hiểu tự nhiên: Tìm hiểu công thức phân tử một số chất trong tự nhiên
– Vận dụng kiến thức, kĩ năng đã học: Nhận biết được hóa trị của nguyên tố trong một hợp chất cộng hóa trị. Biết cách tính hóa trị của nguyên tố trong hợp chất cộng hóa trị. Viết được công thức hóa học của hợp chất , biết cách tính phần trăm nguyên tố trong hợp chất, lập được CTHH dựa vào phần trăm nguyên tố và khối lượng phân tử
Về phẩm chất
– Chăm chỉ, tích cực tham gia hoạt động nhóm phù hợp với khả năng của bản thân;
– Cẩn thận, khách quan và trung thực trong thực hành;
– Có niềm say mê, hứng thú với việc khám phá và học tập khoa học tự nhiên.
THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
– Mô hình nguyên tử, clip mô hình phân tử
– Phiếu học tập
– Các hình ảnh theo sách giáo khoa;
– Máy chiếu, bảng nhóm;
– Phiếu học tập.
Phiếu học tập 1
Câu 1:
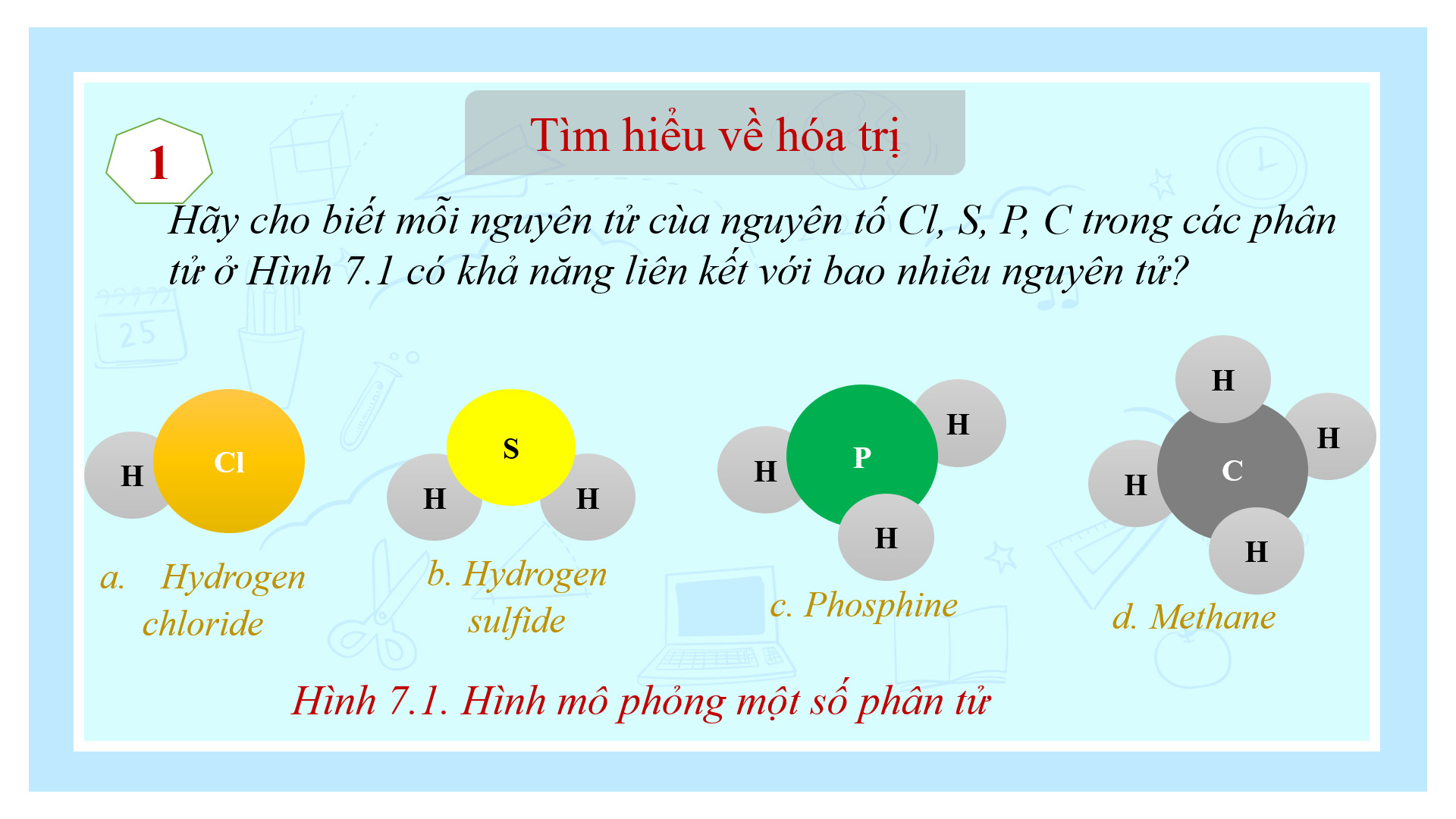
Em hãy cho biết mỗi nguyên tử của nguyên tố Cl, S, P trong các phân tử ở Hình 7.1 có khả năng liên kết với bao nhiêu nguyên tử H
Xác định hoá trị của các nguyên tố Cl, S, P trong các phân tử ở Hình 7.1.
| a.Hydrogen chloride | b. Hydrogen sulfide | c. Phosphine | d. Methane |
| Câu 2: Trong 1 hợp chất cộng hoá trị nguyên tố X có hoá trị IV. Theo em, 1 nguyên tử X có khả năng liên kết với bao nhiêu nguyên tử O hay bao nhiêu nguyên tử H?……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… | |||
PHIẾU HỌC TẬP SỐ 2Câu 1: Hoàn thành bảng sau:
Câu 2: Dựa vào hoá trị các nguyên tố ở bảng Phụ lục 1 trang 187, em hãy cho biết một nguyên tử Ca có thể kết hợp với bao nhiêu nguyên tử Cl hoặc bao nhiêu nguyên tử O.…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. |
PHIẾU HỌC TẬP SỐ 3Câu 1: em hãy hoàn thành bảng sau:
Câu 2: Em hãy hoàn thành bảng sau
Câu 3: Công thức hoá học của iron (III) oxide là Fe2O3, hãy cho biết thành phần nguyên tố, số lượng nguyên tử của mỗi nguyên tố và tính khối lượng phân tử.……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
| PHIẾU HỌC TẬP SỐ 4Câu 1: Tính phấn trăm nguyên tố oxygen trong phân tử nitric acid có công thức hoá học là HNO3.……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….Câu 2: Tính phần trăm mỗi nguyên tố có trong các hợp chất Al2O3, MgCl2, Na2S, (NH4)2CO3.………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………Câu 3: Viết công thức hoá học của phosphoric acid có cấu tạo từ hydrogen và nhóm phosphate, trong phosphoric acid. nguyên tố nào có phần trăm lớn nhất?…………………………………………………………………………………………………………………………….…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. |
PHIẾU HỌC TẬP SỐ 5Câu 1: Hợp chất (Y) có công thức FexOy. Trong đó Fe chiếm 70% theo khối lượng. Khối lượng phân tử (Y) là 160 amu. Xác định công thức hoá học của hợp chất (Y).…………………………………………………………………………………………………………………………….……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….Câu 2: Xác định công thức hoá học của hợp chất sulfur dioxide có cấu tạo từ S hoá trị IV và O.…………………………………………………………………………………………………………………………….………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………Câu 3: Xác định công thức hoá học cùa hợp chất aluminium sulfate có cấu tạo từ Al có hoá trị III và nhóm (SO4) có hoá trị II …………………………………………………………………………………………………………………………….………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………Câu 4: Dựa vào công thức (2), hãy tính hoá trị của nguyên tốa) N trong phân tử NH3.b) S trong phân tử SO2 , SO3c) P trong phân tử P2O5.…………………………………………………………………………………………………………………………….………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………Câu 5: Dựa vào Ví dụ 8,9 và các bảng hoá trị ở Phụ lục trang 187, hãy xác định công thức hoá học các hợp chất tạo bởi: Potassium và sulfat b) Aluminium và carbonate. c) Magnesium và nitrate.…………………………………………………………………………………………………………………………….………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………Câu 6: Dựa vào bảng hoá trị ở Phụ lục trang 187, em hãy hoàn thành bảng sau:
|
III. TIẾN TRÌNH DẠY HỌC
PHƯƠNG PHÁP VÀ KĨ THUẬT DẠY HỌC
Dạy học hợp tác nhóm, cặp đôi.
Dạy học trực quan qua tranh
Dạy học nêu và giải quyết vấn đề thông qua câu hỏi SGK.
Kĩ thuật động não, làm việc với SGK.
HOẠT ĐỘNG DẠY HỌC
Hoạt động 1: Quan sát video – trả lời câu hỏi (15 phút)
a) Mục tiêu: Tạo được hứng thú cho học sinh, Khơi gợi sự tò mò và hứng thú khám phá các chất của học sinh, dẫn dắt học sinh đến với bài học.
b) Nội dung: HS theo dõi video Mô hình cấu tạo của các hợp chất: methane, carbon dioxide, nước
https://www.youtube.com/watch?v=5vy6Q9rsc14
và trả lời các câu hỏi giáo viên đưa ra.
c) Sản phẩm: Học sinh bước đầu nói lên suy nghĩ của bản thân về hóa trị, CTHH
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS | |||
| Quan sát video có trên màn hình máy chiếu và trả lời một số câu hỏi:1. Video trên đang nói đến các mô hình hợp chất nào?2. Từ video và quan sát mô hình phân tử, ta thấy 1 nguyên tử carbon liên kết với 4 nguyên tử hydrogen hoặc chỉ liên kết với 2 nguyên tử oxygen; 1 nguyên tử oxygen liên kết được với 2 nguyên tử hydrogen;… Các nguyên từ liên kết với nhau theo nguyên tắc nào? Bằng cách nào để lập được công thức hoá học của các chất?
|
Học sinh quan sát video và trả lời các câu hỏi của giáo viên đưa ra. | |||
| Giao nhiệm vụ: HS thảo luận để trả lời câu hỏi của GV đưa ra. | Nhận nhiệm vụ | |||
| Hướng dẫn học sinh thực hiện nhiệm vụ: Quan sát, hỗ trợ HS khi cần thiết | Thực hiện nhiệm vụ | |||
| Dẫn dắt HS vào bài |
Hoạt động 2: Tìm hiểu hóa trị, cách xác định hóa trị (30 phút)
Mục tiêu: GV hướng dẫn HS tìm hiểu về hóa trị, cách biểu diễn hóa trị của nguyên tố
Nội dung:
Trong hợp chất cộng hóa trị, các nguyên tử có thể liên kết với nhau bằng liên kết cộng hóa trị. Khả năng liên kết đó được biểu diễn bằng một con số gọi là hóa trị. Vậy làm thế nào có thể xác định hóa trị của một nguyên tố, chúng tuân theo nguyên tác nào, từ nguyên tắc đó ta vận dụng để làm dạng bài tập nào?
GV chia lớp làm 4 nhóm hoàn thành phiếu học tập số 1
Sản phẩm:
Câu 1: a. Em hãy cho biết mỗi nguyên tử của nguyên tố Cl, S, P trong các phân tử ở Hình 7.1 có khả năng liên kết với bao nhiêu nguyên tử H
Xác định hoá trị của các nguyên tố Cl, S, P trong các phân tử ở Hình 7.1.
| a.Hydrogen chloride | b. Hydrogen sulfide | c. Phosphine | d. Methane |
| Cl liên kết với 1 H | S liên kết với 2 H | P liên kết với 3 H | Cliên kết với 4 H |
| Cl hóa trị I | H hóa trị I | P hóa trị III | C hóa trị IV |
| Câu 2: Trong 1 hợp chất cộng hoá trị nguyên tố X có hoá trị IV. Theo em, 1 nguyên tử X có khả năng liên kết với bao nhiêu nguyên tử O hay bao nhiêu nguyên tử H?– X liên kết với 4 nguyên tử H và 2 nguyên tử O | |||
d) Tổ chức thực hiện
| Hoạt động của GV | Hoạt động của HS |
| Giao nhiệm vụ: Chia lớp thành 4 nhóm, yêu cầu các nhóm quan sát Hình 7.1, mô hình phân tử và thảo luận để giải quyết các vấn đề trong phiếu học tập số 1.Câu 1: a. Em hãy cho biết mỗi nguyên tử của nguyên tố Cl, S, P trong các phân tử ở Hình 7.1 có khả năng liên kết với bao nhiêu nguyên tử H b. Xác định hoá trị của các nguyên tố Cl, S, P trong các phân tử ở Hình 7.1.Câu 2: Trong 1 hợp chất cộng hoá trị nguyên tố X có hoá trị IV. Theo em, 1 nguyên tử X có khả năng liên kết với bao nhiêu nguyên tử O hay bao nhiêu nguyên tử H?– Theo em, hóa trị là gì ? – Kết luận, ghi bảng.– Giới thiệu cách xác định hóa trị của 1 nhóm nguyên tử.VD: trong CT H2SO4 , H3PO4 hóa trị của các nhóm SO4 và PO4 bằng bao nhiêu ?– Hướng dẫn HS dựa vào khả năng liên kết của các nhóm nguyên tử với nguyên tử hidrogen | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ– Mỗi nhóm thảo luận kết quả và hoàn thành vào phiếu học tập số 1. | Thảo luận nhóm, hoàn thành phiếu học tập số 1. |
| Báo cáo kết quả: – Cho các nhóm treo kết quả của nhóm mình lên ;– Mời nhóm trưởng đứng vào phần kết quả của nhóm mình;– Gọi 1 nhóm đại diện trình bày kết quả. Các nhóm khác bổ sung– GV kết luận về nội dung kiến thức mà các nhóm đã đưa ra. | – Nhóm xung phong trình bày kết quả ở phiếu học tập;– Nhóm khác nhận xét phần trình bày của nhóm bạn. |
| Tổng kết– Hoá trị của một nguyên tố trong hợp chất là con sổ biểu thị khả năng liên kết của nguyên tử của nguyên tố đó với nguyên tử khác trong phân tử– Hoá trị được biểu diễn bởi số la mã I, II, III… | Ghi nhớ kiến thức |
| Vận dụng-BTVNTrong tự nhiên, Silicon oxide có trong cát, đất sét,… Em hãy xác định hoá trị của nguyên tố Silicon trong Silicon dioxide. Tìm hiểu qua sách báo và internet, cho biết các ứng dụng của hợp chất này. | Học sinh về nhà tìm hiểu và hoàn thành bài tập |
Hoạt động 3: Quy tắc hóa trị. (15 phút)
a) Mục tiêu: HS biết Quy tắc hóa trị, cách vận dụng để biết cách xác định hoá trị nguyên tố, nhóm nguyên tử
b) Nội dung: Tổ chức cho học sinh thao luận cặp đôi, hoàn thành trả lời câu hỏi sau:
3.Em hãy so sánh về tích của hoá trị và số nguyên tử của hai nguyên tố trong phân tử mỗi hợp chất ở Bảng 7.1.
| Chất | Nước | Hydrogen chloride | Aluminium chloride | |||
| Nguyên tố | H | O | H | Cl | Al | Cl |
| Hóa trị | I | II | I | I | III | I |
| Số nguyên tử trong phân tử | 2 | 1 | 1 | 1 | 1 | 3 |
| Tích hóa trị và số nguyên tử | I x 2 | II x 1 | I x 1 | I x 1 | III x 1 | I x 3 |
– Rút ra quy tắc hóa trị
– Luyện tập: Học sinh thảo luận và hoàn thành phiếu học tập số 2
c) Sản phẩm:
Tích của hoá trị và số nguyên tử của hai nguyên tố trong phân tử mỗi hợp chất ở Bảng 7.1 đều bằng nhau
PHIẾU HỌC TẬP SỐ 2Câu 1: Hoàn thành bảng sau:
Câu 2: Dựa vào hoá trị các nguyên tố ở bảng Phụ lục 1 trang 187, em hãy cho biết một nguyên tử Ca có thể kết hợp với bao nhiêu nguyên tử Cl hoặc bao nhiêu nguyên tử O.– 1 nguyên tử Ca có thể kết hợp với 2 nguyên tử Cl– 1 nguyên tử Ca có thể kết hợp với 1 nguyên tử O |
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giao nhiệm vụ: Học sinh thao luận cặp đôi, hoàn thành trả lời câu hỏi sau:
Em hãy so sánh về tích của hoá trị và số nguyên tử của hai nguyên tố trong phân tử mỗi hợp chất ở Bảng 7.1. – Rút ra quy tắc hóa trị– Luyện tập: Chia lớp làm 6 nhóm, phát phiếu học số 2, bảng nhóm, học sinh có 5 phút thảo luận và hoàn thành phiếu học tập |
HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: GV quan sát, hỗ trợ các nhóm khi cần thiết. | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả: – Mời học sinh nhận xét và rút ra quy tắc hóa trị, các bạn khác lắng nghe và bổ sung– Luyện tập:+ Mời các nhóm lên trình bày+ Các nhóm còn lại đưa ra câu hỏi thắc mắc và bổ sung cho nhóm trình bày. | – Các nhóm lần lượt trình bày sản phẩm– Nhóm khác nhận xét, bổ sung phần trình bày của nhóm bạn |
| Tổng kết:Quy tắc hóa trị: Trong phân tử hợp chất hai nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia.Ta có biểu thức: x . a = y . b | HS ghi bài vô vở |
Hoạt động 4: Công thức hóa học của đơn chất (15 phút)
a) Mục tiêu: HS viết được CTHH của đơn chất
b) Nội dung:
– Giáo viên sử dụng phương pháp nêu và giải quyết vấn đề, kĩ thuật công não, động não trả lời các câu hỏi SGK, học sinh lắng nghe và phát vấn
Phân tử của chất được tạo thành từ nguyên tử của một hay nhiều nguyên tố và được biểu diễn bằng công thức hoá học
Công thức hoá học của đơn chất được biểu diễn bằng kí hiệu nguyên tố hoá học kèm với chỉ số ghi ở bên dưới.
– GV cho học sinh quan sát mô hình một số mẫu chất sau:
| Mỗi phân tử có bao nhiêu nguyên tử? Rút ra nhận xét |
GV phân tích ví dụ 2: Phân tử khí hydrogen được tạo thành từ 2 nguyên tử hydrogen liên kết với nhau, công thức hoá học của khí hydrogen là H2
Giáo viên sử dụng kĩ thuật mảnh ghép tổ chức cho học sinh quan sát hình ảnh, tổ chức hoạt động 4 nhóm để ghép được công thức hóa học, tên và khối lượng phân tử phù hợp câu 1 phiếu học tập số 3 và vận dụng hoàn thành phiếu học tập số 3
– Kể tên và viết công thức hoá học các đơn chất kim loại và đơn chất phi kim ở thể rắn.
c) Sản phẩm:
PHIẾU HỌC TẬP SỐ 3Câu 1: Em hãy hoàn thành bảng sau:
|
– Kể tên và viết công thức hoá học các đơn chất kim loại và đơn chất phi kim ở thể rắn.
+ Kim loại sodium có công thức hoá học là Na, kim loại potassium có công thức hoá học là K,…
+ Công thức hoá học của đơn chất carbon, phosphorus, … tương ứng là C, P,…
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giao nhiệm vụ: Học sinh thao luận cặp đôi, hoàn thành trả lời câu hỏi 1 trong phiếu học tập, học sinh có 5 phút thảo luận và hoàn thành phiếu học tậpQuan sát hình 7.2 hoạt động cặp đôi rút ra CTHH của đơn chất | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: Mỗi bàn có 2 bạn sẽ ghép thành một cặp đôi hoàn thành câu 1 PHT số 3Sau khi thảo luận xong, nhóm nào xung phong trình bày và có kết quả tốt sẽ được điểm cộng | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả: – Chọn một cặp đôi lên bảng trình bày– Mời nhóm khác nhận xét– Giáo viên nhận xét sau khi các nhóm đã có ý kiến bổ sung | – Nhóm được chọn trình bày kết quả ở pht– Nhóm khác nhận xét phần trình bày của nhóm bạn |
| Tổng kết:Phân tử của chất được tạo thành từ nguyên tử của một hay nhiều nguyên tố và được biểu diễn bằng công thức hoá họcCông thức hoá học của đơn chất được biểu diễn bằng kí hiệu nguyên tố hoá học kèm với chỉ số ghi ở bên dưới.Công thức hoá học dùng để biểu diễn chất, gồm một hoăc nhiều kí hiệu nguyên tố hoá học kèm với chỉ số ghi ở bên dưới mỗi kí hiệu.Một số đơn chất phi kim thể khí (ở điều kiện thường) Đối với đơn chất kim loại và đơn chất phi kim ở thể rắn | HS ghi bài vô vở |
Hoạt động 4: Công thức hóa học của hợp chất (15 phút)
a) Mục tiêu: HS viết được CTHH của hợp chất, Cách biểu diễn công thức hoá học của hợp chất gồm 2 nguyên tố, tính được phân tử khối.
b) Nội dung: Giáo viên tổ chức cho học sinh hoạt động cặp đôi, làm nhóm để làm rõ nội dung trên
c) Sản phẩm: Phiếu học tập 3
Câu 2: Em hãy hoàn thành bảng sau
| Tên hợp chất | Thành phần phân tử | Công thức hóa học | Khối lượng phân tử |
| Magnesium chloride | 1 nguyên tử Mg và 2 nguyên tử Cl | MgCl2 | 95 |
| Aluminium oxide | 2 nguyên tử Al và 3 nguyên tử O | Al2O3 | 102 |
| Ammonia | 1 nguyên tử N và 3 nguyên tử H | NH3 | 17 |
Câu 3: Công thức hoá học của iron (III) oxide là Fe2O3, hãy cho biết thành phần nguyên tố, số lượng nguyên tử của mỗi nguyên tố và tính khối lượng phân tử.
– Iron (III) oxide gồm 2 nguyên tử Fe và 3 nguyên tử O
– Khối lượng phân tử Iron (III) oxide là: 56 x 2 + 16 x 3 = 160 amu
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giao nhiệm vụ: Giáo viên chia lớp làm 6 nhóm, yêu cầu học sinh quan sát Hình 7.3, vận dụng hoàn thành trả lời câu hỏi 2,3 trong phiếu học tập, học sinh có 7 phút thảo luận và hoàn thành phiếu học tập | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: giáo viên quan sát hỗ trợ các nhóm khi cần thiết Sau khi thảo luận xong, nhóm nào xung phong trình bày và có kết quả tốt sẽ được điểm cộng | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả: các nhóm treo bảng nhóm lên bảng giáo viên đánh giá một số nhóm– Giáo viên giới thiệu thêm cho học sinh một số hợp chất quen thuộc | – Nhóm khác nhận xét phần trình bày của nhóm bạn, giáo viên nhận xét, đânhs giá |
| Tổng kết:– Công thức hóa học dùng để biểu diễn chất, gồm một hoặc nhiều kí hiệu nguyên tố và chỉ số ở bên dưới mỗi kí hiệu.– Công thức chung của phân tử có dạng: AxBy …– Công thức hoá học cho biết thành phần nguyên tố và số lượng nguyên tử của mỗi nguyên tố có trong phân tử đó. Từ đó, có thể tính được khối lượng phân tử.Lưu ý: CÁCH VIẾT CÔNG THỨC HÓA HỌC HỢP CHẤT– Hợp chất tạo bởi oxygen và nguyên tố khác, công thức hoá học có dạng AxOy.– Nếu A là kim loại và B là phi kim, công thức hoá học có dạng AxBy.– Hợp chất tạo bởi hydrogen và nguyên tố A:+ Nếu A thuộc các nhóm IA đến VA, công thức hoá học có dạng AHX. + Nếu A thuộc các nhóm VIA đến VIIA, công thức hoá học có dạng HxA. | HS ghi bài vô vở |
Hoạt động 6: Tính phần trăm nguyên tố trong hợp chất (45 phút)
a) Mục tiêu: Xây dựng công thức tính phần trăm nguyên tố trong hợp chất, vận dụng tính phần trăm nguyên tố trong hợp chất
b) Nội dung: Giáo viên sử dụng kỹ thuật khăn trải bàn tổ chức cho học sinh hoạt độngl àm nhóm để làm rõ nội dung trên
c) Sản phẩm:
| PHIẾU HỌC TẬP SỐ 4Câu 1: Tính phấn trăm nguyên tố oxygen trong phân tử nitric acid có công thức hoá học là HNO3.
Câu 2: Tính phần trăm mỗi nguyên tố có trong các hợp chất Al2O3, MgCl2, Na2S, (NH4)2CO3.Các câu khác tương tự |
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giao nhiệm vụ: Giáo viên chia lớp làm 6 nhóm, yêu cầu học sinh xây dựng công thức tính phần trăm nguyên tố trong hợp chất, vận dụng tính phần trăm nguyên tố trong hợp chất – Hoàn thành phiếu học tập số 4 | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: giáo viên quan sát hỗ trợ các nhóm khi cần thiết Sau khi thảo luận xong, nhóm nào xung phong trình bày và có kết quả tốt sẽ được điểm cộng | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả: các nhóm treo bảng nhóm lên bảng giáo viên đánh giá một số nhóm | – Nhóm khác nhận xét phần trình bày của nhóm bạn, giáo viên nhận xét, đânhs giá |
| Tổng kết:Với hợp chất AxBy , ta có:
Tổng tất cả các phần trăm nguyên tố trong một phân tử luôn bằng 100%. |
HS ghi bài vô vở |
| BTVN: Viết công thức hoá học của phosphoric acid có cấu tạo từ hydrogen và nhóm phosphate, trong phosphoric acid. nguyên tố nào có phần trăm lớn nhất? |
Hoạt động 7: Xác định công thức hoá học dựa vào phần trăm nguyên tố và khối lượng phân tử (20 phút)
a) Mục tiêu: Xác định công thức hoá học dựa vào phần trăm nguyên tố và khối lượng phân tử
b) Nội dung: Giáo viên sử dụng kỹ thuật khăn trải bàn tổ chức cho học sinh hoạt động làm nhóm để xác định công thức hoá học dựa vào phần trăm nguyên tố và khối lượng phân tử, từ đó rút ra các bước xác định công thức hoá học khi biết phần trăm nguyên tố và khối lượng phân tử
Một hợp chất có công thức NxOy trong đó N chiếm 63,64%. Khối lượng phân tử hợp chất là 44 amu. Xác định công thức hoá học của hợp chất
Phân tử X có 75% khối lượng là aluminium, còn lại là carbon. Xác định công thức phân tử của X, biết khối lượng phân tử của nó là 144 amu.
c) Sản phẩm:
Ta có: %O = 100% – %N = 100% – 63,64% = 36,36%
Công thức hoá học của hợp chất là N2O
Gọi công thức hoá học của X là AlxCy.
Ta có: %C = 100% – %Al = 100% – 75% = 25%
Công thức hoá học của hợp chất là Al4C3.
HIẾU HỌC TẬP SỐ 5
Câu 1: Hợp chất (Y) có công thức FexOy. Trong đó Fe chiếm 70% theo khối lượng. Khối lượng phân tử (Y) là 160 amu. Xác định công thức hoá học của hợp chất (Y).
Gọi công thức hoá học của X là FexOy.
Ta có: %C = 100% – %Al = 100% – 70% = 30%
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giáo viên hướng dẫn học sinh cách xác định công thức hoá học của hợp chất dựa vào phần trăm nguyên tố và khối lượng phân tử
Một hợp chất có công thức NxOy trong đó N chiếm 63,64%. Khối lượng phân tử hợp chất là 44 amu. Xác định công thức hoá học của hợp chất 2. Phân tử X có 75% khối lượng là aluminium, còn lại là carbon. Xác định công thức phân tử của X, biết khối lượng phân tử của nó là 144 amu. |
HS lắng nghe giáo viên làm và rút ra các bước xác định CTHH |
| Giao nhiệm vụ: Giáo viên chia lớp làm 4 nhóm, yêu cầu học sinh làm câu 1 phiếu học tập số 5 | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: giáo viên quan sát hỗ trợ các nhóm khi cần thiết Sau khi thảo luận xong, nhóm nào xung phong trình bày và có kết quả tốt sẽ được điểm cộng | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả: các nhóm treo bảng nhóm lên bảng giáo viên đánh giá một số nhóm | – Nhóm khác nhận xét phần trình bày của nhóm bạn, giáo viên nhận xét, đánh giá |
| Đánh giá : Nhóm học sinh làm đúng sẽ GV chấm điểm | |
| Tổng kết: Xác định công thức hoá học khi biết phần trăm nguyên tố và khối lượng phân tử:– Bước 1: Đặt công thức hoá học cần tìm (công thức tổng quát);– Bước 2: Lập biểu thức tính phần trăm nguyên tố có trong hợp chất;– Bước 3: Xác định số nguyên tử của mỗi nguyên tố và viết công thức hoá học cần tìm. | HS ghi bài vô vở |
| Bài tập về nhàPháo hoa có thành phần nhiên liệu nổ gồm sulfur, than và hợp chất (Z). Hợp chất (Z) gồm nguyên tố potassium, nitrogen và oxygen với các tỉ lệ phần trăm tương ứng là 38,61%, 13,86% và 47,53%. Khối lượng phân lử hợp chất (Z) là 101 amu. Xác định công thức hoá học của (Z).Tìm hiếu qua sách, báo và internet, em hãy cho biết một số ứng dụng của hợp chất (Z). | Học sinh về nhà làm |
Hoạt động 8: Xác định công thức hoá học dựa vào quy tắc hóa trị (10 phút)
a) Mục tiêu: Xác định công thức hoá học dựa vào phần trăm nguyên tố và khối lượng phân tử
b) Nội dung: Giáo viên sử dụng kỹ thuật khăn trải bàn tổ chức cho học sinh hoạt động làm nhóm để xác định công thức hoá học dựa vào phần trăm nguyên tố và khối lượng phân tử, từ đó rút ra các bước xác định công thức hoá học khi biết phần trăm nguyên tố và khối lượng phân tử
Một hợp chất có công thức NxOy trong đó N chiếm 63,64%. Khối lượng phân tử hợp chất là 44 amu. Xác định công thức hoá học của hợp chất
Phân tử X có 75% khối lượng là aluminium, còn lại là carbon. Xác định công thức phân tử của X, biết khối lượng phân tử của nó là 144 amu.
c) Sản phẩm:
| HIẾU HỌC TẬP SỐ 5Câu 2: Xác định công thức hoá học của hợp chất sulfur dioxide có cấu tạo từ S hoá trị IV và O.– Công thức hoá học chung là – Theo quy tắc hóa trị, ta có: x. IV = y . II– Chuyển thành tỉ lệ: – Vậy x = 1, y = 2– Công thức hoá học của hợp chất này là SO2Câu 3: Xác định công thức hoá học cùa hợp chất aluminium sulfate có cấu tạo từ Al có hoá trị III và nhóm (SO4) có hoá trị II – Công thức hoá học chung là Alx(SO4)y– Theo quy tắc hóa trị, ta có: x x III = y x II– Chuyển thành tỉ lệ: – Vậy x = 2, y = 3– Công thức hoá học của hợp chất này là Al2(SO4)3Câu 4: Dựa vào công thức (2), hãy tính hoá trị của nguyên tố
N trong phân tử NH3. – Công thức hoá học chung là – Theo quy tắc hóa trị, ta có 1 x a = 3 x I → a=3– Vậy hóa trị của N là III.b) S trong phân tử SO2 , SO3
c) P trong phân tử P2O5.– Công thức hoá học chung là – Theo quy tắc hóa trị, ta có 2 x a = 5 x 2 → a=5– Vậy hóa trị của P là V. |
d) Tổ chức thực hiện:
| Hoạt động của GV | Hoạt động của HS |
| Giáo viên cho học nhắc lại quy tắc hóa trịCTHH:Ta có biểu thức: x . a = y .b (2)GV hướng dẫn học sinh cách lập CTHH từ ví dụCâu 2 phiếu học tập số 5: Xác định công thức hoá học của hợp chất sulfur dioxide có cấu tạo từ S hoá trị IV và O. | HS lắng nghe giáo viên làm và rút ra các bước xác định CTHH, vận dụng làm bài tâpk |
| Giao nhiệm vụ: Giáo viên chia lớp làm 4 nhóm, yêu cầu học sinh làm Câu 3 PHT số 5Nhóm 1: Tính hoá trị của nguyên tố N trong phân tử NH3.Nhóm 2: Tính hoá trị của nguyên tố S trong phân tử SO2 Nhóm 3: Tính hoá trị của nguyên tố S trong phân tử SO3Nhóm 4: Tính hoá trị của nguyên tố P trong phân tử P2O5. | HS nhận nhiệm vụ. |
| Hướng dẫn HS thực hiện nhiệm vụ: giáo viên quan sát hỗ trợ các nhóm khi cần thiết Sau khi thảo luận xong, nhóm treo kết quả lên bảng, đại diện các nhóm trình bày và có kết quả tốt sẽ được điểm cộng, nhóm khác nhận xét, bổ sung | Phân công nhiệm vụ và tiến hành thực hiện nhiệm vụ. |
| Báo cáo kết quả– Chọn đại diện lên bảng trình bày– Mời nhóm khác nhận xét– Giáo viên nhận xét sau khi các nhóm đã có ý kiến bổ sung | – Nhóm trình bày kết quả – Nhóm khác nhận xét phần trình bày của nhóm bạn |
| Đánh giá : Nhóm học sinh làm đúng sẽ GV chấm điểm | |
| Tổng kết: Xác định công thức hoá học dựa vào quy tắc hoá trị:– Bước 1: Đặt công thức hoá học cần tìm (công thức tổng quát).– Bước 2: Lập biếu thức tính dựa vào quy tắc hóa trị, chuyển thành tỉ lệ các chỉ số nguyên tử.– Bước 3: Xác định số nguyên tử (những số nguyên đơn giản nhất, có tỉ lệ tối giản) và viết công thức hoá học cần tìm. | HS ghi bài vô vở |
| Bài tập về nhà: Bột thạch cao có nhiều ứng dụng quan trọng trong đời sống. Thành phần chính của bột thạch cao là hợp chất (M) gồm calcium và gốc sulfate. Xác định công thức hoá học cùa hợp chất (M).Tìm hiếu thông qua sách, báo, internet và cho biết các ứng dụng của thạch cao. | Học sinh về nhà làm |
Hoạt động 7: Luyện tập (10 phút)
Mục tiêu: Học sinh sử dụng kiến thức đã học để học sinh trả lời được câu hỏi sgk
Nội dung: Học sinhhoàn thành phiếu học tập số 5:
Câu 5: Dựa vào Ví dụ 8,9 và các bảng hoá trị ở Phụ lục trang 187, hãy xác định công thức hoá học các hợp chất tạo bởi:
Potassium và sulfat
b) Aluminium và carbonate.
c) Magnesium và nitrate.
Câu 6: Dựa vào bảng hoá trị ở Phụ lục trang 187, em hãy hoàn thành bảng sau:
| Chất | Công thức hóa học | Khối lượng phân tử |
| Sodium sulfide (S hóa trị II) | ||
| Aluminium nitride (N hóa trị III) | ||
| Copper (II) sulfate | ||
| Iron (III) hydroxide |
Sản phẩm: PHT
Câu 5: Dựa vào Ví dụ 8,9 và các bảng hoá trị ở Phụ lục trang 187, hãy xác định công thức hoá học các hợp chất tạo bởi:
Potassium và sulfat
– Công thức hoá học chung là
– Theo quy tắc hóa trị, ta có: x. I = y. II
– Chuyển thành tỉ lệ: x/y = II/I= 2/1. Vậy x = 2, y = 1
– Công thức hoá học của hợp chất này là K2SO4
Câu 6: Dựa vào bảng hoá trị ở Phụ lục trang 187, em hãy hoàn thành bảng sau:
| Chất | Công thức hóa học | Khối lượng phân tử |
| Sodium sulfide (S hóa trị II) | Na2S | 78 |
| Aluminium nitride (N hóa trị III) | AlN | 37 |
| Copper (II) sulfate | CuSO4 | 160 |
| Iron (III) hydroxide | Fe(OH)3 | 107 |
Tổ chức thực hiện
| Hoạt động của giáo viên | Hoạt động của học sinh |
| Giao nhiệm vụ:giáo viên chia lớp 4 nhóm, thảo luận trả lời câu hỏi PHT số 3 | Nhận nhiệm vụ |
| Hướng dẫn thực hiện: giáo viên quan sát hỗ trợ các nhóm khi cần thiết | Làm bảng nhóm |
| Báo cáo kết quả : các nhóm treo bảng nhóm lên bảng giáo viên đánh giá một số nhóm | Theo dõi đánh giá giáo viên |
| Đánh giá: nhóm nào làm đúng, nhanh giáo viên đánh giá cho điểm cho các nhóm. |
Hoạt động 8: Vận dụng (5 phút)
Mục tiêu: Học sinh biết vận dụng kiến thức để trả lời câu hỏi thực tế
Nội dung: Học sinh tham gia trò chơi “nhanh như chớp”. với 11 câu hỏi
Câu 1: Người ta quy ước gán cho H hóa trị mấy?
Câu 2: Hóa trị của Al trong công thức hóa học Al2O3 là
Câu 3: Hóa trị của nhóm CO3 trong công thức H2CO3
Câu 4: Công thức hóa học của Ca(II) với OH(I) là
Câu 5: Hóa trị của C trong CO biết Oxygen hóa trị là II
Câu 6: Hóa trị của N trong các hợp chất sau: NO, NO2, N2O5 lần lượt là
Câu 7: Hóa trị của S trong công thức SO2 là
Câu 8: Xác định hóa trị của Fe trong các hợp chất sau: FeO, Fe2O3?
Câu 9: Trong MgO, Mg có hóa trị là
Câu 10: Hóa trị của nhóm SO4 trong công thức H2SO4 là
Câu 11: Công thức hóa học H2Cl đúng hay sai?
Sản phẩm: Phiếu trả lời câu hỏi của học sinh
Tổ chức thực hiện
| Hoạt động của giáo viên | Hoạt động của học sinh |
| Thông báo luật chơi: Luật chơi– 2 đội chơi, mỗi đội 3 thành viên. – Mỗi đội có 1 bộ câu hỏi, trả lời trong thời gian 2 phút.– Đội nào trả lời nhiều câu hỏi đúng, nhanh nhất sẽ là đội chiến thắng và cho điểm từng nhóm. | Ghi nhớ luật chơi |
| Giao nhiệm vụ: Học sinh quan sát câu hỏi và trả lời nhanh nhất có thể . | Giao nhiệm vụ |
| Hướng dẫn thực hiện nhiệm vụ: | Thực hiện nhiệm vụ |
| Báo cáo kết quả: Tổng kết điểm các nhóm và thưởng |
DẶN DÒ
Học sinh làm bài tập sách giáo khoa, sách bài tập
Chuẩn bị bài mới trước khi đến lớp.